Мочекаменная болезнь занимает одно из первых мест среди урологических заболеваний в России (в среднем 34,2%) [1]. Хотя причины возникновения мочекаменной болезни (МКБ) до конца не изучены, известно, что наряду с индивидуальными особенностями физиологии (и метаболизма) человека ей способствует также факторы неблагоприятной среды обитания (экология, пища и т.д.), что характерно для крупных индустриальных городов.
Для лечения мочекаменной болезни традиционно применяют следующие методы: хирургическая операция, ультразвуковое измельчение камня, медикаментозное растворение и т.д. Однако удаление почечного конкремента без последующей коррекции рациона питания (диеты) больного более чем в половине случаев приводит к рецидиву мочекаменной болезни [2]. Для назначения соответствующей диеты необходима информация о минеральном составе камней как о долговременной характеристике существующей патологии мочевыделительной системы конкретного пациента.
Данная работа посвящена исследованию урологических камней различными физико-химическими методами с целью выявления закономерности процессов их образования, а также способов предотвращения как первичного, так и повторного развития мочекаменной болезни. В качестве объектов для исследования были выбраны уролиты пациентов, проживающих в бассейне реки Обь и ее притоков. Для населенных пунктов в данном районе характерна высокая антропогенная нагрузка. Кроме того, ранее уже проводились исследования фазового и элементного состава почечных камней из Новосибирской [3,4], Омской [5-7] и Челябинской областей [8,9]. Однако, выборки объектов в данных работах были небольшими, порядка 100-150 образцов. Представляется интересным исследование изменения фазового и микроэлементного состава в течение 10-15 лет на примере данных субъектов Российской Федерации.
Обсуждение результатов
В таблице 1 показано распределение образцов для рентгенофазового анализа (РФА) для городов расположенных вдоль реки Обь и на ее основных притоках. Разница в количестве образцов не означает большую заболеваемость в том или ином регионе, но только отражает, сколько образцов удалось отобрать для анализа. К тому или иному типу (оксалаты, фосфаты, мочевая кислота и ее соли) относятся почечные камни, в фазовом составе которых содержится более 50% соответствующего компонента.
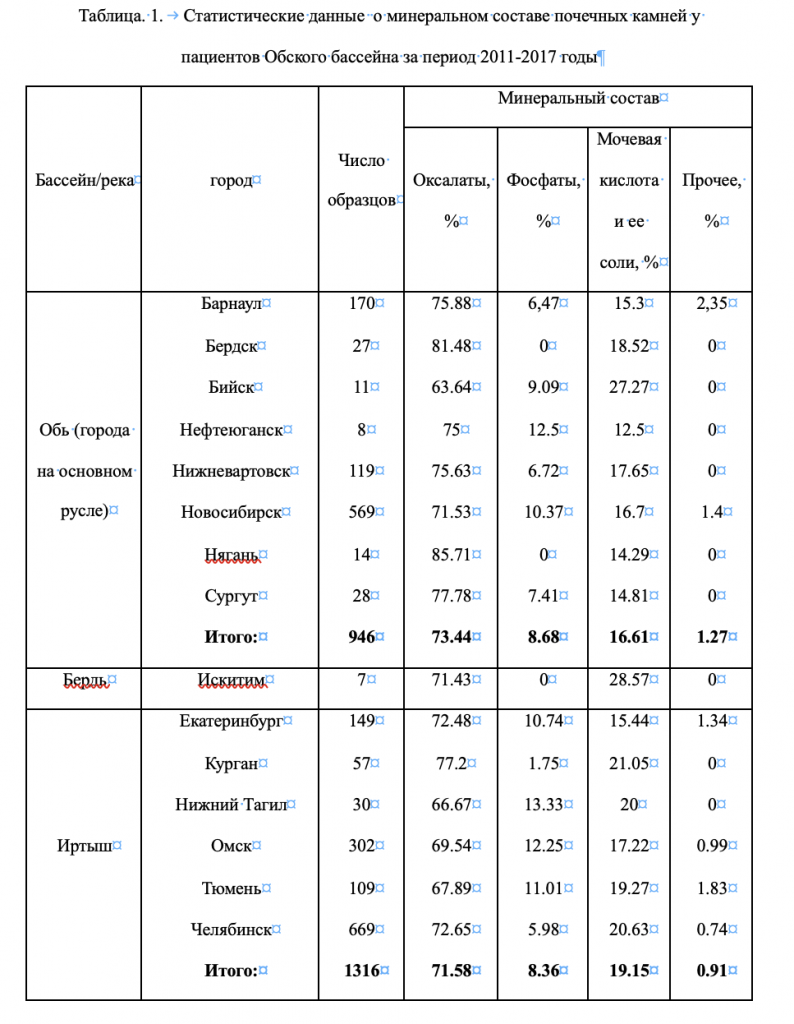
Наиболее часто встречаются оксалаты: вевеллит СаС2O4·(1+х)H2O (х ≈ 0,00 – 0,07) и ведделлитCаC2O4·(2+х)H2O (х ≈ 0,13-0,37); фосфаты: cтрувит MgNH4PO4·6H2O, гидроксилапатит Ca5(PO4)3(OH), брушит CaHPO4·2H2O; мочевая кислота и ее соли: урикит (мочевая кислота) C5H4N4O3, дигидрат мочевой кислоты C5H4N4O3·2H2O, урат аммония (NH4)2C5H2N4O3. Значительно реже попадаются почечные камни, состоящие из цистина C6H12N2O4S2, кварца SiO2, кальцита СаСО3.
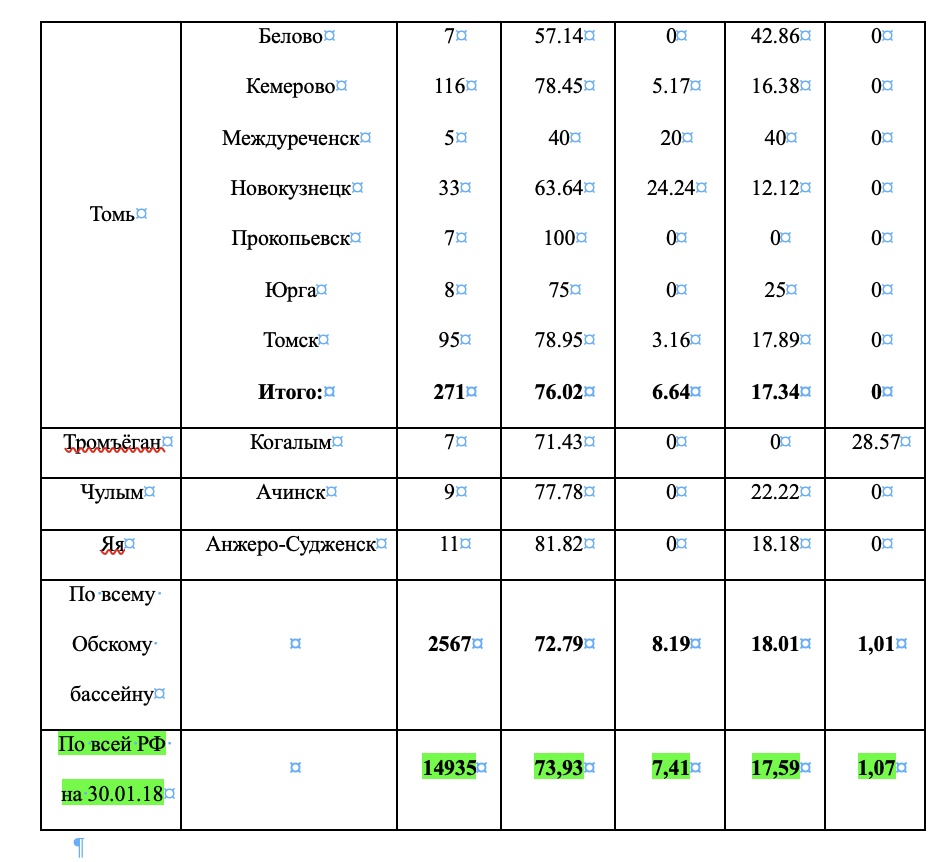
В среднем, по всему Обскому бассейну доля оксалатов составляет 73 % от всех урологических камней, мочевая кислота и ураты – 18 %, фосфаты – 8 %. 1 % образцов приходится на смеси, содержащие равное число основных компонентов и образцы, состоящие из таких редких фаз, как цистин, кварц, гипс и т.д. (см. табл. 1). В трех наиболее представительных (по количеству образцов) регионах соотношение незначительно варьируется. Так, в Новосибирской и Омской областях чаще встречаются фосфаты – 10-12 %, в Челябинской – мочевая кислота и ее соли (21 %). Ранее, в монографии Головановой О.А. [7], была исследована выборка из 155 почечных камней из Новосибирской области и 129 камней из Омской области. Было установлено, что в Омской области оксалаты встречаются в 57,7 % случаев, фосфаты – 23,7 %, мочевая кислота и ее соли – 18,6 %. В Новосибирске: оксалаты - 65,7 % случаев, фосфаты – 23,5 %, мочевая кислота и ее соли – 10,8 %. Таким образом, за прошедшие 10 лет серьезно изменился состав почечных камней. В Омской области более чем на 10% выросло число оксалатов и соответственно сократилось число фосфатов и мочевой кислоты. В Новосибирской области на 5-7% выросло число оксалатов и мочевой кислоты. На 13% уменьшилось количество фосфатов.
Опубликованы данные от 2004 года по составу почечных камней 112 коренных жителей Южного и Среднего Урала [10]. Часть данных территорий относится к Обскому бассейну, как и Челябинская область. В работе показано, что оксалаты встречаются в 61 % случаев, мочевая кислота и ее соли – 23,6 %, фосфаты – 14,7 %. Нами было исследовано 669 образцов из Челябинска. Найдено: оксалаты – 73 %, мочевая кислота и ее соли – 21 %, фосфаты – 6 %. Как и в случае Новосибирской и Омской областей, наблюдается рост количества оксалатов более чем на 10%. Можно предположить, что данные изменения не связаны с локальными изменениями условий жизни, а являются следствием более глобальных причин. Возможно, это связано с изменением характера потребляемых продуктов и политикой импортозамещения, проводимой в Российской Федерации.
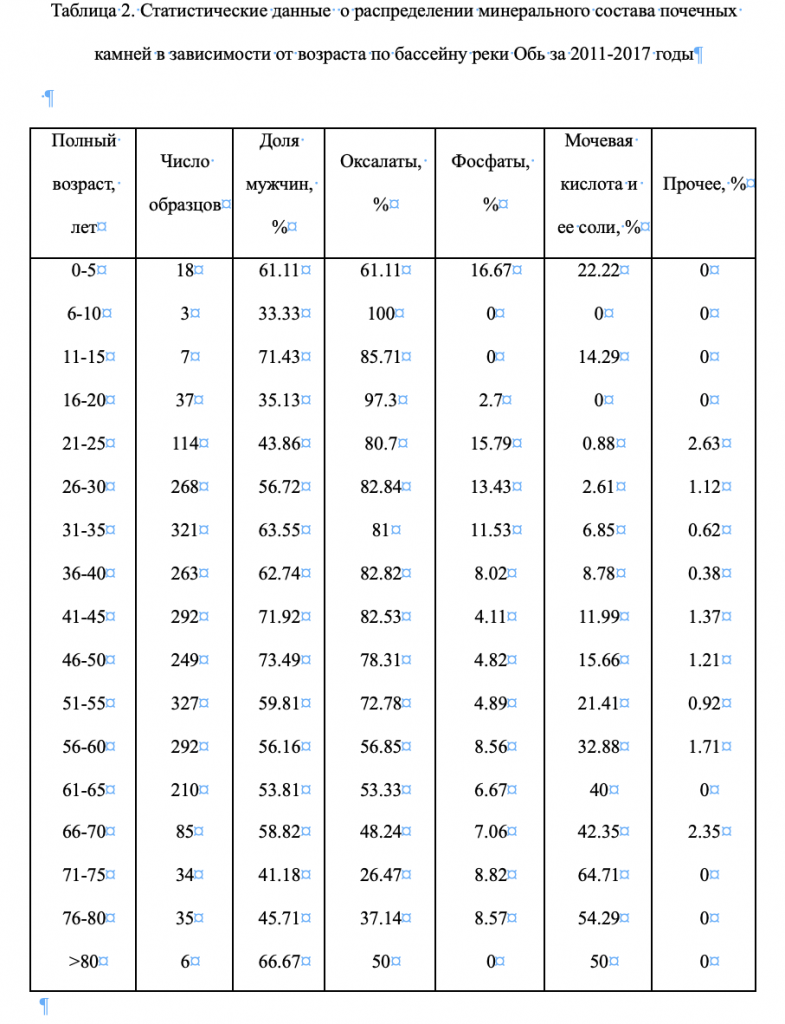
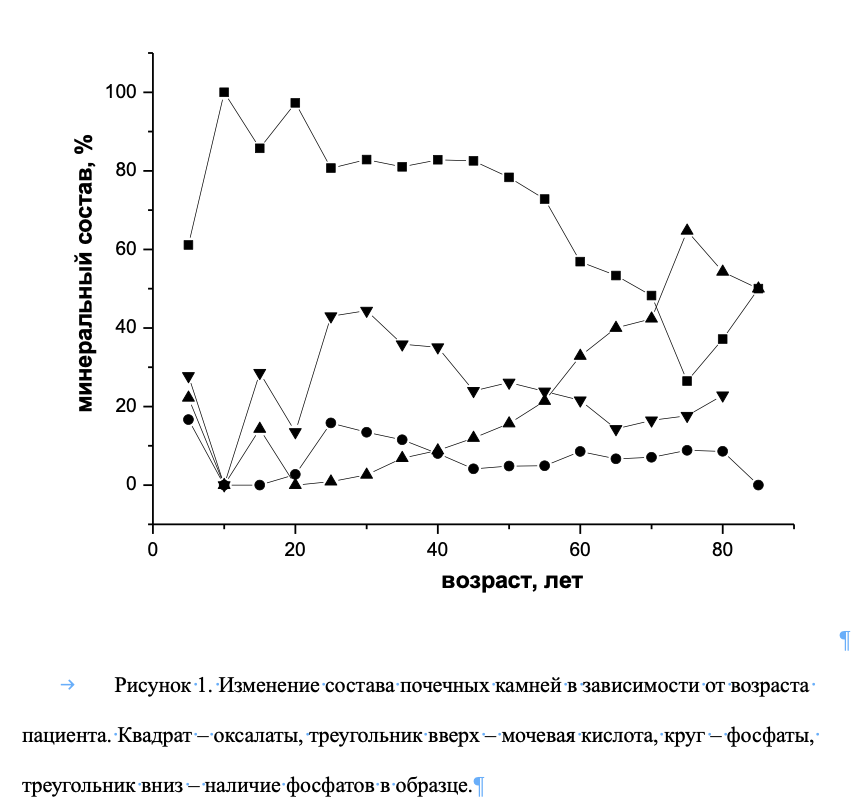
Представляется интересным проследить изменение соотношения типов почечных камней в зависимости от возраста пациента. Наибольшее количество образцов представлено для пациентов от 21 до 70 лет (см. табл. 2.). Из рисунка 1 видно, что с возрастом растет количество больных с почечными камнями, состоящими из мочевой кислоты и ее солей: от 1 % в 21-25 лет до 65 % в 71-75 лет. При этом падает число больных с оксалатными камнями: с 81 % в 21-25 лет до 26 % в 71-75 лет. Количество пациентов с фосфатными камнями так же падает: с 16 % в 21-25 лет до 9 % в 71-75 лет. На рис. 1. представлена динамика количества образцов, содержащих любое количество фосфатов в составе (линия голубого цвета). Видно, что пик содержания фосфатов приходится на возраст 25 – 40 лет. Максимум доли фосфатных камней (т.е. содережащих более 50% вес. Фосфатов) так же приходится на период 20-35 лет, то есть период активной половой жизни и, скорее всего, связан с мочеполовыми инфекциями. Считается, что генезис фосфатных камней связан с инфекционными заболеваниями [11].
По данным атомно-эмиссионной спектроскопии (АЭС), кроме основных элементов (Ca, P, Mg, Na, K), содержащихся в макроколичествах (более 0,1 % вес.), был найден ряд микроэлементов (0,001 – 0,1 % вес): Ba, Bi, Cd, Cr, Cu,Co, Fe, Mn, Mo, Ni, Re, Rb, Si, Sr, Ta, Zn, Pb, Al, W.
Во всех 9 образцах, состоящих, по данным РФА, только из минералов оксалатного типа, обнаружен фосфор. Содержание фосфора в этих камнях варьируется от 0,71 до 4,5 % вес. Это дает основания полагать о наличии в уролитах минералов фосфатного типа в рентгеноаморфном состоянии, что подтверждается литературными данными [12-14]. Авторы статей указывают, что продукты жизнедеятельности приводят к образованию аморфных фосфатов, либо, при наличии ядра кристаллизации, ускоряют рост конкрементов. Кроме этого, во всех оксалатных камнях обнаружено содержание Na (0,13 – 1,8 % вес.), Mg (0,02 – 0,52 % вес.), K(0,021 – 0,12 % вес.). На уровне 0,001 – 0,1 % вес часто встречаются Zn, Sr и Fe. Реже – Pb, Mo, W.
Как и в случае оксалатных камней, в фосфатных образцах содержится Na (0,17 – 3 % вес.), K(0,022 – 0,57 % вес.). На уровне 0,001 – 0,1 % вес. во всех образцах обнаружены Zn и Sr. Реже встречаются Fe, Mo, Ba.
Методом АЭС среди камней, состоящей из мочевой кислоты, крайне редко удается обнаружить макроэлементы с содержанием более 1%. Среди 15 исследованных образцов в одном случае было найдено 10 % вес. Ca. По-видимому, фазы, включающие данные элементы находятся в рентгеноаморфном состоянии. На уровне 0,1 – 1 % вес встречаются Na, Ca, K, P. В одном из образцов найдено 0,62 % вес. Si, в другом – 0,22 % вес. Мо. В целом, среди уратов найдено больше всего различных микроэлементов. На уровне 0,001 – 0,1 % вес. найдены: Fe, Ta, Mo, Al, Bi, Zn, W, Pb, Cu, Rb, Cd.
Исследователи расходятся во мнении, что является основополагающим фактором, определяющим микроэлементный состав почечного камня. Некоторые связывают состав с регионом проживания пациента [15], другие – с фазовым составом образцов [16]. В целом, сопоставление литературных данных в данной области затруднительно из-за различий применяемых методов исследования состава и спектра анализируемых микроэлементов.
Экспериментальная часть
Изучение фазового состава почечных камней размером 2 мм и более проводили на порошковых дифрактометрах Shimadzu XRD-7000 и ДРОН-3М (CuKa излучение, кремниевый монохроматор на отраженном пучке, диапазон 5 – 50° 2q, шаг 0.03° 2q, накопление 1 с). Образцы для исследования готовили следующим образом: конкременты истирали в агатовой ступке в присутствии гептана; полученную суспензию наносили на полированную сторону стандартной кварцевой кюветы; после высыхания гептана образец представлял собой тонкий ровный слой (толщина ~100 мкм). Индицирование дифрактограмм проводили по данным картотеки PDF[17]. Количественный РФА проводили методом корундовых чисел.
Анализ микроэлементного состава проводили с использованием атомно-эмиссионного спектрометра с индуктивно связанной плазмой iCAP-6500 Duo (Thermo Scientific) с различными видами пневматической системы ввода растворов в индуктивно-связанную плазму. Управление спектрометром и обработку аналитических данных производили с помощью программы iTEVA. Для анализа методом АЭС было выбрано 36 образцов с различным минеральным составом. Из них 17 образцов с мономинеральным составом, из которых 3 оксалатных камня, 3 фосфатных, 9 - мочевая кислота и 2 камня, состоящих полностью из цистина. Остальные 19 камней были с полиминеральным составом.
На примере Новосибирской, Омской и Челябинской областей показано, что за 10-15 лет произошли существенные изменения в фазовом составе почечных камней. На 10 % вес. увеличилось число оксалатных камней, на 5-10 % сократилось число фосфатных конкрементов. Между самими областями наблюдаются незначительные различия в составе образцов конкрементов: в Новосибирской и Омской областях чаще встречаются фосфаты – 10-12 %, в Челябинской – мочевая кислота и ее соли (21 %).
Был исследован элементный состав 36 камней методом АЭС. Выявлено наличие фосфора в камнях оксалатного типа, которые, по данным РФА не содержат фосфатов. Содержание фосфора в этих камнях варьируется от 0,71 до 4,5 % вес. По данным АЭС, кроме основных элементов (Ca, P, Mg, Na, K), содержащихся в макроколичествах (более 0,1 % вес.), был найден ряд микроэлементов (0,001 – 0,1 % вес): Ba, Bi, Cd, Cr, Cu, Co, Fe, Mn, Mo, Ni, Re, Rb, Si, Sr, Ta, Zn, Pb, Al, W. Для оксалатов характерно наличие Na, Mg, K. В меньших концентрациях встречаются Zn, Sr, Fe. Для фосфатов – Na, K, Zn, Sr. Для камней, состоящей из мочевой кислоты: Na, Ca, K, P. В одном из образцов найдено 0,62 % вес. Si, в другом – 0,22 % вес. Мо. В целом, среди мочевой кислоты и ее солей найдено больше всего различных микроэлементов, не обнаруженных в других типах камней: Ta, Al, Bi, Cu, Rb, Cd.
Работа выполнена при поддержке Российского фонда фундаментальных исследований (грант № 18-45-540008).
Авторы статьи: И.В. Корольков,1,2,@ А.И. Губанов,1,2 Е.Ю. Филатов,1,2 А.Р. Цыганкова1,2
1 Институт неорганической химии им. А.В. Николаева, 630090, Россия, Новосибирск, пр. Лаврентьева, 3
2 Новосибирский государственный университет, факультет естественных наук, 630090, Россия, Новосибирск, ул. Пирогова, 2
E-mail: korolkov@niic.nsc.ru
Список литературы
1. Аляев Ю.Г., Руденко В.И., Газимиев М.-С.А. Мочекаменная болезнь. Актуальные вопросы диагностики и выбора метода лечения. М.-Тверь: ООО «Издательство «Триада», 2006. 236с.
2. Левковский С.Н. Мочекаменная болезнь: прогнозирование течения и метафилактика. Санкт-Петербург: ООО «Типография «Береста», 2010. 120с.
3. Голованова О.А., Пятанова П.А., Пальчик Н.А., Столповская В.Н., Григорьева Т.Н., Низовский А.И., Шкуратов С.С. // Химия в интересах устойчивого развития. 2003. Т. 11. Вып. 4. С. 593.
4. Голованова О.А., Пальчик Н.А., Максимова Н.В., Дарьин А.В. // Химия в интересах устойчивого развития. 2007. Т. 15. Вып. 1. С. 55.
5. Голованова О.А., Очкасова Е.Ю., Пятанова П.А. // Вестник Санкт-Петербургского университета. 2005. Сер. 7. Вып. 4. С. 87-92.
6. Бельская Л.В., Голованова О.А., Лемешева С.А. // Вестник Омского университета. 2006. Вып. 3. С. 26-27.
7. Голованова О.А. // Известия ВУЗ. 2004. T 47. Вып. 1. С. 3-12.
8. Максимова Н.В., Дарьин А.В., Золотарев К.В., Сокол Э.В., Нигматулина Е.Н., Чиглинцев А.Ю. // Поверхность, рентгеновские, синхротронные и нейтронные исследования. 2003. Вып. 12. С. 49-52.
9. Чиглинцев А.Ю. // Materials digest of the XLV International Research and Practice Conference and I stage of the Championship in medicine and physical culture, pharmaceutics. International Academy of Science and Higher Education. 2013. P. 104-105.
10. Нигматулина Е.Н., Сокол Э.В., Максимова Н.В., Чиглинцев А.Ю., Я.Л. Лукьянов Я.Л. // Химия в интересах устойчивого развития. 2004. Т. 12. С. 67-81.
11. Е.Т. Голощапов, А.В. Четвериков, Е.С. Белозеров // Урологические ведомости. 2016. T 6, Вып. 4, с. 21-27. DOI: 10.17816/uroved6421-27.
12. Аль-Шукри С.Х., Голощапов Е.Т., Эмануэль Ю.В., Горбачев М.И. // Саратовский научно-медицинский журнал. 2011. T 7. Вып. S2. С. 108-109.
13. Ченина И.Н., Неймарк А.И., Неймарк Б.А. // Эксп. и клин. урология. 2010. Вып. 4. С. 30-31.
14.Baumann JM., Affolter B., Meyer R. // Urol. res. 2010. V.38. № 1. P. 21-27. DOI: 10.1007/s00240-009-0239-8
15. Полиенко А.К. Автореф. дис. канд. геол.-минерал. наук. Л., 1986. 21 с.
16. Тыналиев М.Т. Почечнокаменная болезнь: (избранные проблемы нефролитиаза в Киргизии). Фрунзе: Мектеп, 1990. 176с.
17. Powder Diffraction File, PDF-2, International Centre for Diffraction Data, Pennsylvania, USA, 2010.
